
神经递质的精准、稳定活体监测是解析大脑功能及神经疾病机制的重要基础。电化学适配体传感器因具备分子识别特异性强、响应可逆、无需外加试剂等优势,成为活体神经化学分析的重要技术路径。然而,现有传感器多依赖天然构型的D-DNA适配体,其在体内易受核酸酶降解,同时界面构象稳定性有限,通常只能稳定工作数小时,难以满足长时程神经动态监测需求。如何在保持分子识别能力的同时显著提升体内稳定性,是该领域亟待突破的关键科学问题。
北京师范大学化学学院江迎教授团队长期围绕“识别元件分子工程”与“识别元件—电极界面偶联化学”两大核心问题开展系统研究。一方面,通过分子结构理性设计提升识别元件在复杂生理环境中的选择性、响应动力学与构象可控性;另一方面,构建稳定可控的碳基微电极表界面修饰与共价偶联体系,实现识别分子的定向固定与电信号高效耦联,推动核酸基电化学传感器在脑化学信号活体原位测量中的应用(Angew. Chem. Int. Ed. 2020, 59, 18996;Angew. Chem. Int. Ed. 2022, 61, e202208121;Angew. Chem. Int. Ed. 2025, 64, e202501701)。
近期,针对适配体在体内易降解及界面失稳的瓶颈问题,团队从分子结构与界面化学双层面提出协同优化策略:通过手性反转构建镜像核酸(L-DNA)识别元件以增强抗酶降解能力,同时优化其与碳基电极之间的共价偶联路径与界面电子传递结构,构建出高生物稳定性、界面结构可控的镜像核酸–电极表界面体系,为活体长期稳定监测奠定化学基础。
以神经递质多巴胺为例,研究团队将其D型适配体进行手性反转,构建对应的L型镜像适配体。研究发现,在保持原有空间折叠特征的前提下,L型适配体仍可有效识别非手性小分子多巴胺,无需重新筛选即可获得功能性识别单元(图1)。这一结果为非手性小分子靶标的镜像适配体构建提供了新的可行路径。
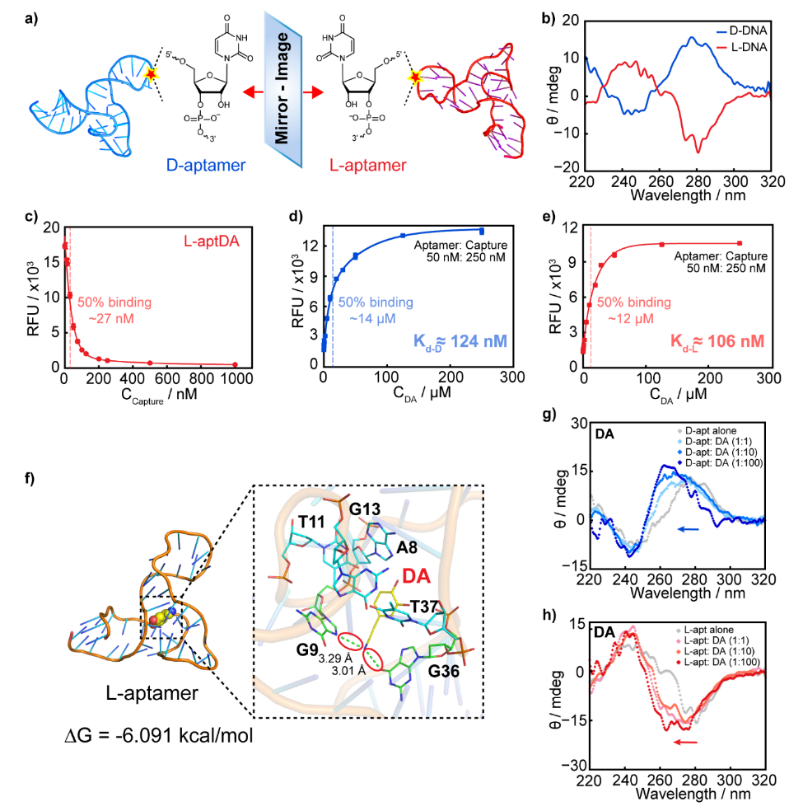
图1. 镜像L-型适配体的设计及表征
在此基础上,团队将镜像适配体与稳定化电化学界面策略相结合,构建了基于镜像核酸的多巴胺活体电化学传感平台。动物实验表明,该传感器在大鼠脑内连续工作24小时后仍保持约85%的信号响应,而传统D型适配体传感器信号已衰减至10%以下(图2)。结果表明,镜像核酸策略可显著提升电化学适配体传感器在体内环境中的长期稳定性,为长时程神经递质动态监测提供了重要技术支撑。
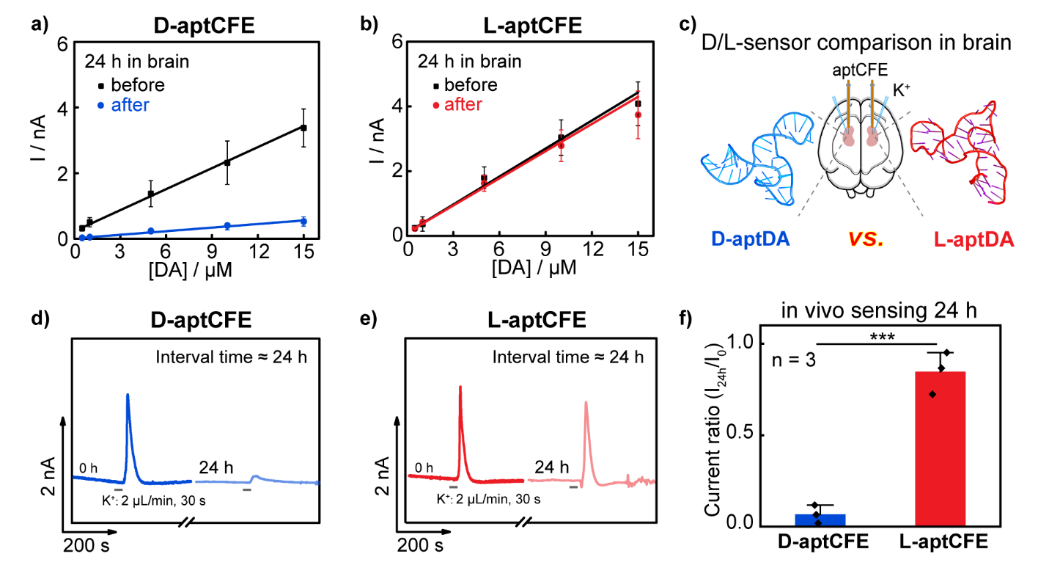
图2. 镜像L-型与传统D-型传感器稳定性对比
该研究从分子手性设计出发,将镜像核酸识别单元与电化学稳定化界面协同整合,形成了“分子结构调控—界面化学优化”相结合的新思路,为镜像核酸在复杂生物环境中的分析应用拓展了新的方向。
该研究近期以“Mirror-Image L-DNA Aptamers Enable Stable In Vivo Dopamine Sensing”为题发表于Journal of the American Chemical Society。通讯作者为江迎教授,北京师范大学化学学院为唯一通讯单位。文章第一作者是化学学院博士研究生刘瀛寰(2025级)和靳莹(2021级)。本研究得到中央高校基本科研业务费、国家自然科学基金项目及国家重点研发计划资助。


