线粒体Ca2+摄取过程参与细胞多种基础生命活动,例如刺激ATP的产生、调控细胞代谢、缓冲胞浆Ca2+浓度等等。研究表明线粒体钙离子摄取主要通过位于线粒体内膜上的具有高Ca2+亲和性和选择性的单向转运体(uniporter)通道完成。单向转运体亚基缺失或者表达异常会导致脑神经发育障碍、骨骼肌肌肉萎缩以及学习运动障碍等多种疾病,因此细胞内钙稳态对维持正常生命活动至关重要。
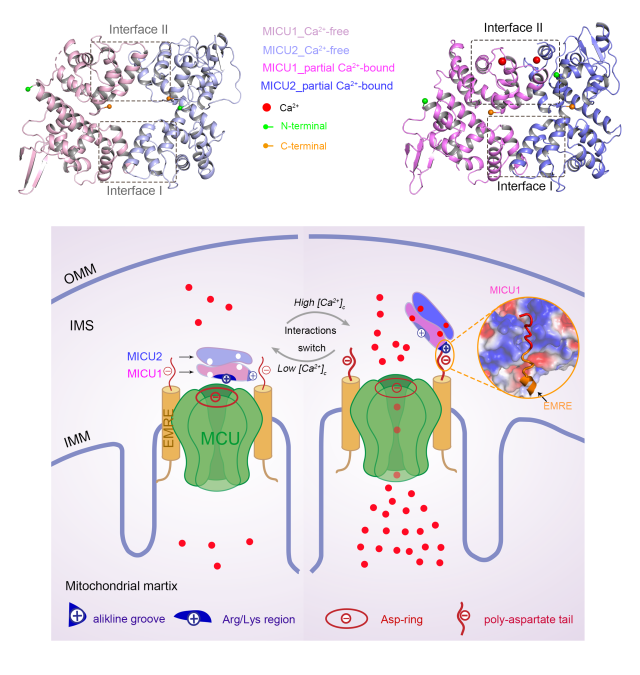
单向转运体Ca2+摄取阈值是由钙结合蛋白MICU1和MICU2共同调控的,均含有两个经典的EF-hand钙离子结合功能域。郑积敏老师课题组长期关注uniporter的研究,2019年课题组在EMBO Reports报道了MICU2的Ca2+-bound状态的三维结构。但是由于线粒体钙离子摄取体系的复杂性,钙离子的摄取机制仍旧不清楚。课题组在此研究的基础上,继续探究了MICU1-MICU2复合物的结构与功能,成功的解析出了Ca2+-free和partial Ca2+-bound两种状态的复合物的三维结构,复合物结构显示出“面对面”反平行排列的相互作用模式。通过比对两种状态MICU1-MICU2复合物的结构,揭示了其从apo到holo状态构象的变化过程。通过蛋白表面电荷分析以及微量热涌动(MST)实验鉴定了MICU1-MICU2与桥连蛋白EMRE之间的相互作用是通过MICU1蛋白的碱性口袋与EMRE的酸性C末端静电相互作用结合,并且此相互作用是钙离子依赖型,即在有钙离子存在的情况下相互作用增强。然而MICU1-MCU在无钙离子情况下相互作用增强,因此MICU1与MCU和EMRE相互转换的结合模式帮助钙离子信号完成了从调控亚基传递到离子通道,同时也揭示了MICU1-MICU2复合物 “门控”和“协同激活”两种相反功能的转换机制。最后,课题组利用外源EMRE C末端多肽竞争细胞内源EMRE,结果表明EMRE多肽降低了静息状态下MCU钙离子摄取的阈值,同时增加了刺激状态下线粒体内钙离子的积累。
这项研究工作最近被欧洲分子生物学会杂志(EMBO Journal)发表,北京师范大学化学学院为第一完成单位,化学学院郑积敏教授课题组博士生吴文萍和沈庆亚为论文的共同第一作者。该研究得到国家自然科学基金资助,特此感谢!